
研究速览
最近,北京大学和济南大学在《ADVANCED SCIENCE》期刊发表了多酶模拟氮化钼纳米酶通过活性氧调控与微生物组重塑重塑龈下微环境用于协同牙周炎治疗。牙周炎是由菌斑微生物与宿主免疫反应引发的慢性炎症,是全球失牙主要原因。传统机械清创与抗生素、消毒剂辅助治疗因牙周解剖结构复杂、耐药性、龈下渗透与滞留差等问题疗效有限。本研究设计了一种具有过氧化物酶、氧化酶、过氧化氢酶三重模拟酶活性的 Mo-N 配位纳米酶(Mo₅N₆)。依托 Mo-N 配位与多酶模拟特性,该纳米酶可动态调控龈沟内局部氧化反应,在有效杀伤致病菌的同时避免过度氧化应激;高效清除对活性氧(ROS)敏感的厌氧革兰氏阴性牙周致病菌,减轻致病刺激。该策略不仅改善牙周微环境,还能促进共生菌群恢复与牙周组织再生,证实Mo₅N₆纳米酶在牙周炎治疗中具有重要应用潜力。
要点分析
要点一:材料设计与多酶催化特性
研发Mo₅N₆拟氮化钼纳米酶,通过一步退火法合成,具备过氧化物酶 (POD)、氧化酶(OXD)、过氧化氢酶(CAT)三重模拟酶活性;依托Mo-N配位结构与介孔高比表面积,可在牙周微环境中精准调控ROS生成与清除,酸性条件下高效产生活性氧杀菌,中性/弱碱性下分解过量 H₂O₂避免组织氧化损伤,催化稳定性与底物亲和力优于天然酶与多数纳米酶。
要点二:牙周炎协同治疗机制与效果
抗菌与破生物膜:联合低浓度H₂O₂可高效杀灭牙龈卟啉单胞菌、具核梭杆菌等牙周致病菌,深度清除龈下生物膜,效果媲美临床3%H₂O₂且安全性更高;微环境重塑:抑制破骨细胞、减少牙槽骨吸收,促进巨噬细胞向抗炎M2型极化,下调促炎因子、上调抗炎因子;微生物组调控:恢复龈下菌群α/β多样性,减少致病菌丰度,富集双歧杆菌、唾液乳杆菌等有益菌,重建共生微生态;生物安全性:体外细胞毒性低、无溶血风险,体内主要器官无病理损伤,具备临床转化潜力。
图文导读
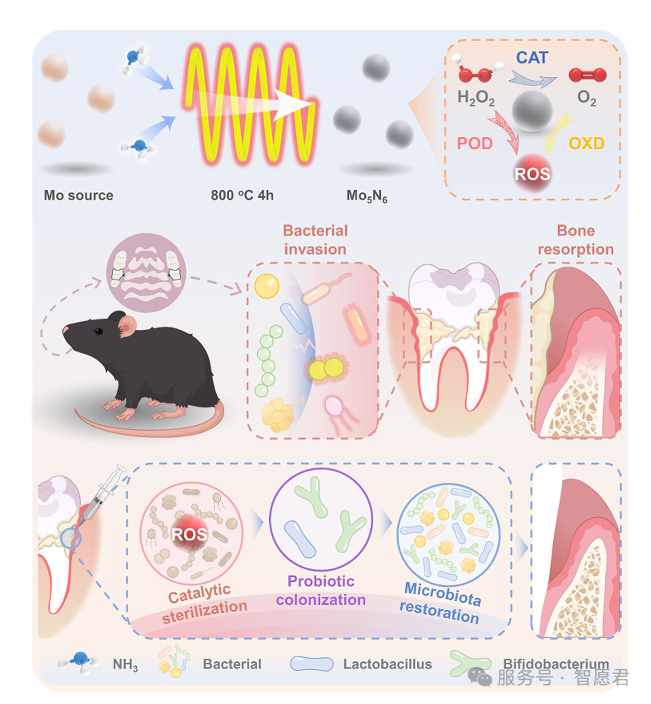
方案一.五氮化五钼纳米酶的合成示意图及其对牙周炎的治疗机制
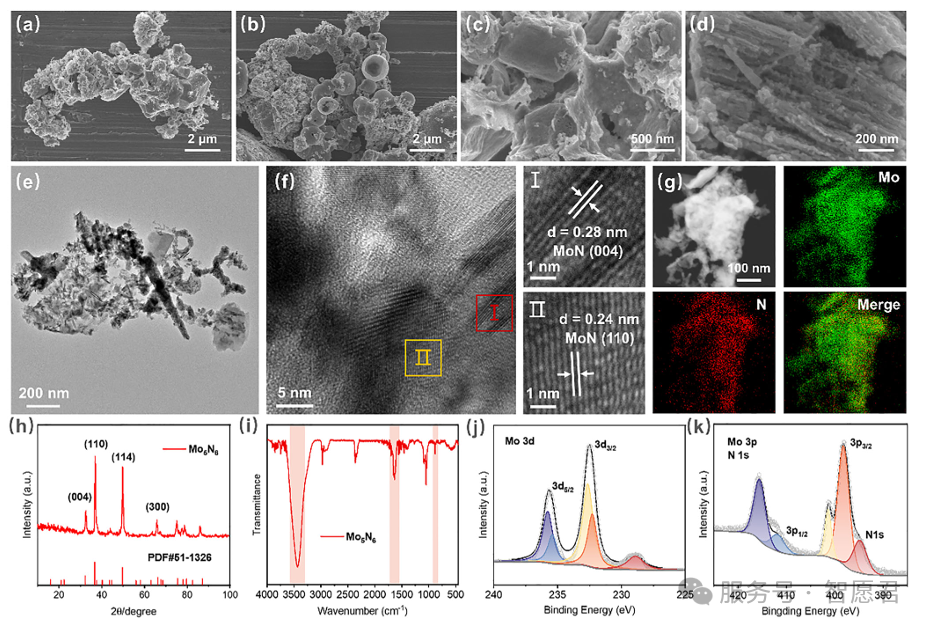
图1.五氮化六钼(Mo₅N₆)的合成与表征。(a–d) 五氮化六钼的扫描电子显微镜(SEM)图像,(e) 透射电子显微镜(TEM)图像,(f) 高分辨透射电子显微镜(HRTEM)图像以及(g)能谱分析(EDS)图像。(h)五氮化六钼的X射线衍射(XRD)图谱及其标准图谱。(i) 五氮化六钼的傅里叶变换红外光谱(FTIR)。(j)五氮化六钼的钼3d轨道X射线光电子能谱(XPS)与(k)氮1s轨道X射线光电子能谱。
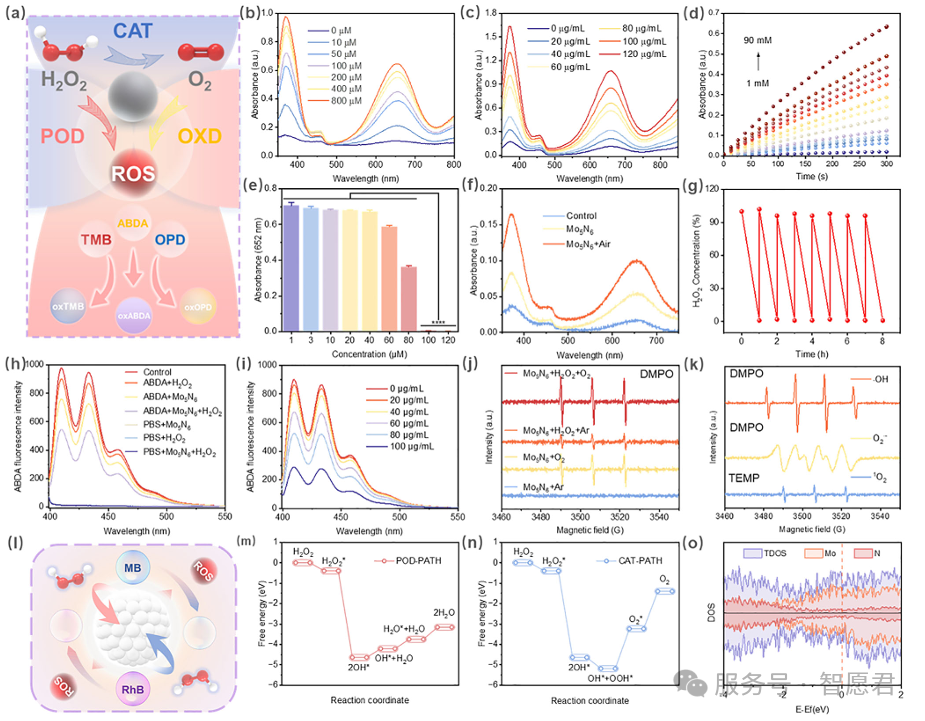
图 2. Mo₅N₆纳米酶的活性氧(ROS)生成性能。(a) 过氧化氢分解反应机理以及 3,3',5,5'- 四甲基联苯胺(TMB)、1,3 - 二苯基异苯并呋喃(ABDA)与邻苯二胺(OPD)氧化反应机理。不同 (b) 过氧化氢浓度与 (c) Mo₅N₆浓度下氧化型 TMB 的吸光度。(d) 不同 TMB 浓度下 Mo₅N₆类过氧化物酶(POD)活性在 652 nm 处随时间变化的吸光度曲线。(e) 加入不同浓度抗坏血酸(AA)后 652 nm 处的终点吸光度。(f) 不同反应条件下通过类过氧化物酶活性生成的氧化型 TMB 的紫外 - 可见吸收光谱。(g) 循环稳定性测试中过氧化氢消耗量的定量结果(催化循环定义为:在催化剂用量恒定的条件下,过氧化氢完成一次完整的氧化还原反应,每次反应后补加新鲜过氧化氢)。Mo₅N₆在连续 9 次循环后仍保留 96.1% 的催化活性。(h) 不同反应条件与 (i) 梯度浓度下 ABDA 的紫外 - 可见吸收光谱。(j) 可控催化条件下生成单线态氧(¹O₂)的电子顺磁共振(EPR)谱;以及采用不同自旋捕获剂检测 (k) 羟基自由基(・OH)、超氧阴离子自由基(O₂・⁻)与单线态氧(¹O₂)的电子顺磁共振谱:其中 5,5 - 二甲基 - 1 - 吡咯啉 - N - 氧化物(DMPO)用于检测・OH 与 O₂・⁻,2,2,6,6 - 四甲基哌啶(TEMP)用于检测 ¹O₂。(l) 亚甲基蓝(MB)与罗丹明 B(RhB)降解机理示意图。(m) 类过氧化物酶反应路径的自由能曲线,展示过氧化氢吸附、氧 - 氧键断裂及含OH 中间体的形成过程。(n) 类过氧化氢酶(CAT)反应路径的自由能曲线,显示过氧化氢通过OOH/*O₂中间体逐步歧化为氧气与水的过程。(o) Mo 的 d 轨道与 N 的 p 轨道的总态密度(TDOS)与分波态密度(PDOS),费米能级设为 0 eV(虚线)。数据显著性采用单因素方差分析计算。ns:无显著性差异,*p < 0.05,p < 0.01,*p < 0.001,p < 0.0001。
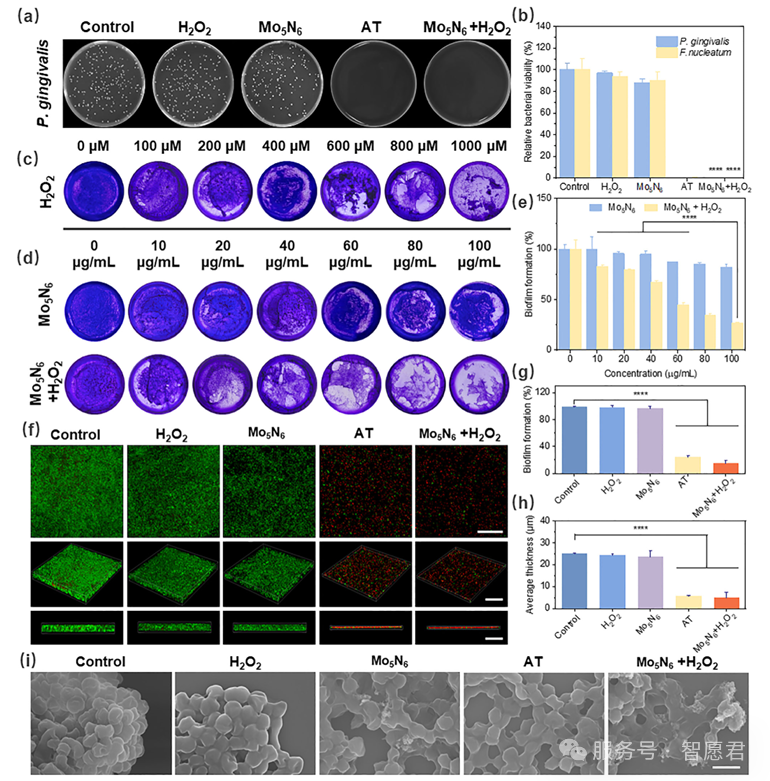
图 3. Mo₅N₆对牙龈卟啉单胞菌(Pg)的体外抗菌性能评价。五组牙龈卟啉单胞菌的对比结果如下:未处理对照组(Control)、仅经 200 μM 过氧化氢(H₂O₂)或 100 μg/mL Mo₅N₆处理组(Mo₅N₆)、3% 过氧化氢处理组(阳性处理组,AT)以及 100 μg/mL Mo₅N₆与 200 μM 过氧化氢联合处理组(Mo₅N₆+H₂O₂)。(a) 牙龈卟啉单胞菌形成的菌落照片。(b) 采用平板计数法测定的牙龈卟啉单胞菌相对存活率。(c) 经不同浓度过氧化氢处理后细菌生物膜的结晶紫染色图像。(d) 在有无过氧化氢处理条件下,不同材料浓度作用下牙龈卟啉单胞菌生物膜的结晶紫染色图像。(e) 通过结晶紫染色在 595 nm 光密度(OD₅₉₅)下定量牙龈卟啉单胞菌生物膜的生物量。(f) 不同处理后牙龈卟啉单胞菌生物膜的三维共聚焦激光扫描显微镜(CLSM)活 / 死染色图像(标尺:50 μm)。(g) 图 (f) 中生物膜生物量及 (h) 平均厚度的统计学分析。
(i) 牙龈卟啉单胞菌的扫描电子显微镜(SEM)图像(标尺:1 μm)。数据以 n=3 的平均值 ± 标准差(mean±SD)表示。采用单因素方差分析(one-way ANOVA)进行数据显著性检验。ns:无显著性差异,*p<0.05,p<0.01,*p<0.001,p<0.0001。
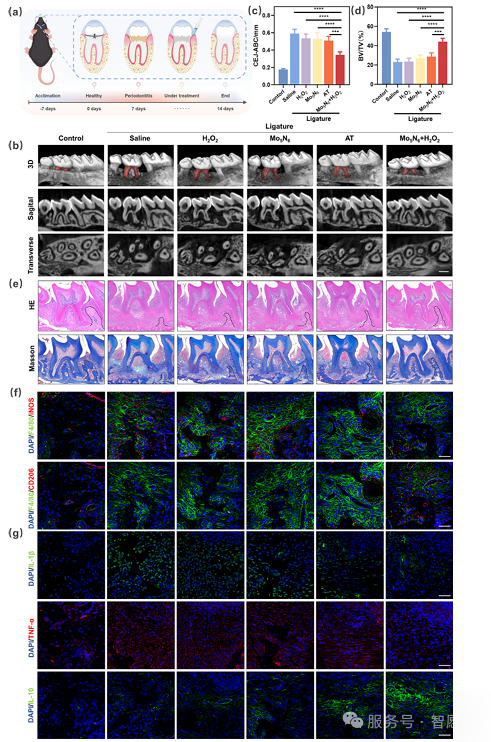
图 4. Mo5 N6 干预对牙周炎诱导的牙槽骨吸收的体内抑制作用。(a) 丝线结扎诱导牙周炎模型及治疗流程示意图。(b) 小鼠治疗后第二磨牙周围单侧上颌骨代表性三维重建及二维显微 CT 可视化图像(比例尺:500 微米)(n=8)。(c) 牙骨质釉质界至牙槽骨嵴顶的距离,用以反映牙槽骨吸收程度(n=8)。(d) 骨体积分数(BV/TV)定量分析,反映矿化骨组织占总组织体积的比例(n=8)。(e) 牙周组织苏木精 - 伊红染色及马松染色图像(比例尺:400 微米)。(f) 小鼠牙周组织中 M1 型与 M2 型巨噬细胞标志物的代表性免疫荧光染色图像(比例尺:50 微米)(n=3)。(g) 小鼠牙周组织中炎症因子的代表性免疫荧光染色图像(比例尺:50 微米)(n=3)。数据以平均值 ± 标准差表示。数据显著性采用单因素方差分析计算。ns:无统计学差异,*p<0.05,p<0.01,*p<0.001,p<0.0001。
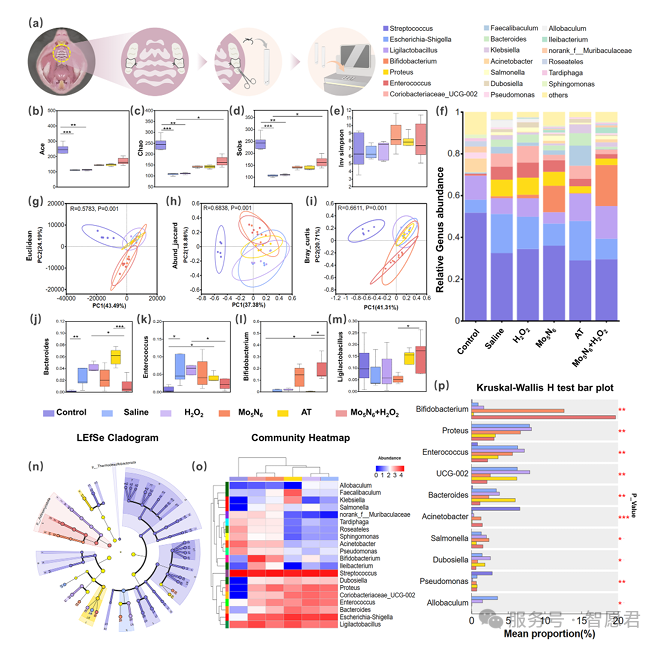
图 5. Mo5 N6 处理对龈下微生物群落结构的调控作用。(a) 牙周微生物组 16S rDNA 分析的取样流程示意图。(b–e) 通过 Ace、Chao、Sobs 和 Inv simpson 分析对龈下微生物组进行 α 多样性分析(每组 n=5,Wilcoxon 秩和检验)。(f) 各组在属水平上龈下微生物群落相对丰度的堆叠箱线图。分别采用 (g) 欧氏距离、(h) 丰度‑贾卡德距离和 (i) 布雷‑柯蒂斯相异度进行主坐标分析(PCoA),以评估 β 多样性并可视化处理诱导的微生物群落结构变化(每组 n=5,PERMANOVA 检验)。(j–m) 牙周区域中 (j) 拟杆菌属、(k) 肠球菌属、(l) 双歧杆菌属和 (m) 敏捷乳杆菌属的相对丰度分析(每组 n=5,Wilcoxon 秩和检验)。(n) 采用 LEfSe 分析展示不同组中优势菌(门至属水平),LDA 值>2。各节点的直径与颜色表示其在对应组中的富集程度。(o) 热图展示 20 种优势菌在不同样本中的相对丰度分布(属水平),横坐标为组别名称,纵坐标为科水平细菌分类学信息。不同颜色梯度(从蓝色至红色)表示相对丰度大小。顶部与左侧的聚类树状图反映丰度模式的相似性关系。(p) 各类微生物丰度比较(每组 n=5,Wilcoxon 秩和检验)。数据以 n=5 的平均值 ± 标准差表示。ns:无显著性差异,*p<0.05,p<0.01,*p<0.001,p<0.0001。
结论
该研究成功研发出具备过氧化物酶、氧化酶、过氧化氢酶三重模拟酶活性的 Mo₅N₆ 氮化钼纳米酶,依托Mo-N配位结构与介孔高比表面积,可在牙周微环境中精准、动态调控ROS生成与清除,实现杀菌与抗氧化损伤的平衡。该纳米酶联合低浓度 H₂O₂可高效杀灭牙周致病菌、深度破坏龈下生物膜,显著抑制牙槽骨吸收、促进牙周软组织修复,并推动巨噬细胞向抗炎 M2 型极化,缓解慢性炎症。纳米酶能重塑龈下微生物组,恢复菌群多样性,减少有害菌、富集双歧杆菌等有益菌,重建口腔共生微生态,降低牙周炎复发风险。Mo₅N₆ 纳米酶生物相容性优异,无明显细胞毒性与体内器官损伤,提出了“ROS杀菌+益生菌定植”的协同牙周炎治疗新策略,具备临床转化潜力。
全文链接:https://doi.org/10.1002/advs.202517770








